רשתית
תבנית אנטומיה ריקה
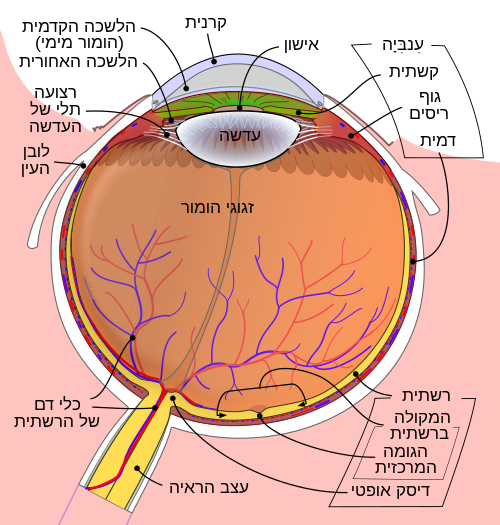

הרשתית (בלטינית ובאנגלית: retina - מהמילה הלטינית ל"רשת" rete) היא שכבת תאים דקה הצמודה לחלקו האחורי של גלגל העין של בעלי החוליות וכמה חסרי חוליות. זהו החלק בעין שממיר אור לאותות עצביים במה שמכונה מסלול ה-phototransduction (אנ').[1]

הרשתית מכילה תאים קולטי אור: קנים ומדוכים, תאים דו-קוטביים ותאי גנגליון שעליהם נופל האור שמרכזת עדשת העין. הפוטורצפטורים מתמירים את האור לאותות עצביים, מהם עובר האות אל התאים הדו-קוטביים ומשם אל תאי הגנגליון. מתאי הגנגליון האותות עוברים אל המוח הגדול באקסונים היוצרים את עצב הראייה, באמצעות פוטנציאלי פעולה . עצב הראייה (עצב גולגולגת מס' 2) הוא אוסף הסיבים העצביים של תאי הגנגליון ברשתית.
תפקיד הרשתית אינו מצומצם לגילוי אור בלבד - כבר בתוכה מתבצע עיבוד ראשוני של הקלט הראייתי. לפיכך, היא ממלאת תפקיד ביצירת התפיסה החזותית.
בשל אופן יצירתה של הרשתית בתהליך ההתפתחות העוברית של המוח, הרשתית נחשבת חלק ממערכת העצבים המרכזית.
המבנה הייחודי של כלי הדם ברשתית משמש לזיהוי ביומטרי.
אנטומיה של הרשתית
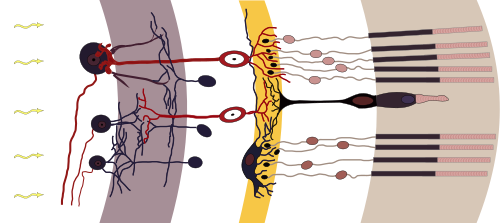
הרשתית של עין האדם בנויה מעשר שכבות שונות, שרשומות להלן בסדר הולך ומתקרב אל הקרנית:
---קרוב לשכבה דמית ולממברנת ברוק (Bruch's Membrane)---
- אפיתל פיגמנט הרשתית (RPE) - (אנ') (שכבה של תאי גלייה התומכת בפוטורצפטורים מכיוון הדמית)
- שכבת פוטורצפטורים - קנים ומדוכים
- ממברנה מגבילה חיצונית - שכבה שמפרידה את שכבות הפיגמנט הפנימיות של הפוטורצפטורים מגרעיני התא שלהן.
- שכבה גרעינית חיצונית - של תאי הפוטורצפטורים
- שכבת פלקסיפורם חיצונית - באזור המקולה. ידועה כשכבת הסיבים של הֵנלֵה בה נפגשים אקסוני הפוטורצפטורים עם דנדריטים של תאים הוריזנטליים ובי פולאריים
- שכבה גרעינית פנימית - תאים הוריזנטליים, אמקרינים ובי פולאריים
- שכבת פלקסיפורם פנימית - בה נפגשים אקסוני התאים הבי פולאריים עם דנדריטים של תאי הגנגליון
- שכבת תאי גנגליון (GCL – Ganglion cell layer) - מכילה גרעיני תאי גנגליון וממנה יוצאים סיבי העצב האופטי.
- שכבת סיבי העצב - צבר של כמיליון האקסונים היוצא כעצב הראייה
- ממברנה מגבילה פנימית - בה מתחילים תאי מילר (Müller glia (אנ')) המגיעים עד לתחילת שכבת הפוטורצפטורים
---קרוב לגוף הזגוגי (Vitreous Humour) ולקרנית---
שכבה חיצונית הכוונה שהיא פונה מאחור (anterior) העין, היינו יותר קרובה לדמית, לעומת פנימית שהיא קדמית (posterior), היינו יותר קרובה לקרנית . מכאן נובע ששכבות הרשתית שקופות לאור עד שזה נפגש בפוטורצפטורים, הנמצאים למעשה כמעט בקצה גלגל העין.
מבנה רשתית האדם
ברשתית יש שלוש שכבות תאים. השכבה הראשונה היא של תאים קולטי אור. השנייה היא של תאי עצב, שמקשרת בין תאים אלו לתאי גנגליוני הרשתית, שגופם יוצר את השכבה השלישית, והאקסונים שלהם יוצרים את עצב הראייה, המוביל את מידע הראייה למוח.[3]
שכבת התאים קולטי האור
בעין האדם הנורמטיבי יש חמישה סוגי תאים קולטי אור, שבכל אחד מהם סוג חלבון קולט אור, בשם אופסין, שייחודי לו. הסוג הראשון הוא זה שמזהה את כמות האור הנכנסת לעין, כדי להרחיב או לצמצם את הקשתית, ולשלוט בכמות האור הנכנסת. הסוג השני הוא האופסין של תאי הקנים. שלושת הסוגים האחרים הם של שלושת סוגי תאי המדוכים.

בסך הכול יש בעין כשישה מיליון מדוכים וכ-125 מיליון קנים. אלה מצופפים על גזרה של 72% משפת כדור שקוטרו 22 מ"מ, באדם בוגר. במרכז הרשתית נמצא העצב האופטי, המכונה "הכתם העיוור" (Blind spot) היות שאין בו תאים קולטי אור. זהו אזור אליפטי שצבעו לבן, בשטח כ-3 מ"מ רבועים. מצד הכתם העיוור, בכיוון הרקות נמצא הכתם שבמרכזו הגומה המרכזית. הגומה המרכזית מרוצפת בכוורת צפופה במיוחד של מדוכים קטנים ביותר, בסידור משושה המאפשר ניצולת מרבית של פני השטח ללא שטחים מתים. הצפיפות המשטחית של המדוכים בגומה המרכזית מגיעה לכ-140,000 מדוכים למילימטר רבוע. כך מושגת חדות ראייה מרבית בגומה המרכזית, על חשבון רגישות פחותה לאור קלוש.
הגומה המרכזית (אנגלית: Fovea(אנ')) (לטינית: fovea centralis) היא חלק הממוקם במרכז אזור המקולה ברשתית שבחלק האחורי של העין. הגומה אחראית לראיה המרכזית בה משתמשים בני אדם לקריאה, צפייה בטלוויזיה, ולכל פעולה אחרת הדורשת הבחנה טובה בפרטים. צפיפות המדוכים בפוביאה היא הגדולה ביותר, ולמעשה שם ראיית הצבע היא הטובה ביותר, וכן גם חדות הראייה היא הטובה ביותר.
סביב הגומה נמצאים אזורים הקרויים פאראפוביאה, ופריפוביאה. הפאראפוביאה היא אזור בצורת טבעת שבו שכבת תאי הגנגליון מורכבת מיותר מחמש שורות של תאים. הפריפוביאה היא האזור המקיף את הפאראפוביאה ובו אותה שכבה מורכבת רק משתיים עד ארבע שורות. באזורים אלו חדות הראייה פחותה מאשר בתוך הגומה ממש. מסביב לגומה מצוי אזור גדול יותר שבו חדות הראיה נמוכה.
לבני אדם ולפרימטים גומה מרכזית יחידה בעין, בניגוד למיני ציפורים מסוימים, כגון נץ שלהם גומה כפולה או לכלבים ולחתולים שאין להם גומה מרכזית אלא פס מרכזי של פוטורצפטורים. ברדיוס של שישה מ"מ מסביב לגומה המרכזית נמצא מרכז הרשתית. האזור שמרוחק יותר נקרא שולי הרשתית.
ככל שמתרחקים מן הגומה המרכזית לכיוון שולי הרשתית, צפיפות המדוכים יורדת ושכיחות הקנים עולה. בזווית של כעשרים מעלות ביחס לקו הראייה מגיעה צפיפות הקנים לשיא של כ-160,000 קנים למילימטר רבוע. היות ששיעור קטן יותר של תאי גנגליון מוקדשים לעיבוד המידע משולי הרשתית, רגישות העין לאור היא מרבית בהיסט קטן יותר: 8-16 מעלות ביחס לקו הראייה.Averted Vision, web.archive.org, 2007-03-28 אסטרונומים המחפשים גרמי שמיים חיוורים משתדלים להביט מעט הצידה ממקומו המשוער, כדי להיעזר ברגישות המוגברת של העין לאור בזוויות אלה. שיטה זו נקראת ראייה מופנית (Averted vision).
מבנה הרשת העצבית
המדוכים והקנים מתעצבבים לתאי עצב דו-קוטביים (ביפולריים), שסיביהם העצביים שלוחים לעבר תאי גנגליון. תא עצב דו-קוטבי רשתיתי יוצר סינפסות עם תאי קנים או עם תאי מדוכים, אך לא עם שניהם יחד. הוא מקבל קלט עצבי גם מתאי עצב אופקיים, התורמים להשפעה ההדדית בין תאי עצב סמוכים וכך עשויים לשפר את רגישות העין או את חדות הדמות שנוצרת ברשתית העין. תאי אמקרין מעורבים בהתכנסות האותות הבאים מתאי קנה סמוכים שנמצאים בהיקף הרשתית, ובכך, תורמים לרגישות הראיה. כ־1.2 מיליון סיבים עצביים של תאי הגנגליון מתאגדים לעצב הראייה, הנושא את המידע שנקלט ועובד מכ-130 מיליון תאים קולטי אור. מכאן שהסוגים השונים של תאי העצב ברשתית נדרשים לדחוס ולסנן את הקלט האורי, לשם קידודו לדחפים עצביים הנשלחים בסיבים העצביים המרכיבים את עצב הראייה.
בחתך צד עוביה של הרשתית אינו עולה על חצי מ"מ. יש בה שלוש שכבות של תאי עצב ושתי שכבות של סינפסות. העצב האופטי מקשר את האקסונים של תאי הגנגליון אל המוח, שם מתבצע עיבוד התמונה. תאי הגנגליון הם שכבה פנימית ברשתית בעוד שהתאים הרגישים לאור הם שכבה חיצונית (רחוקה יותר מעדשת העין). בגלל מבנה זה האור עובר דרך שכבות הרשתית לפני שהוא פוגע בקנים ובמדוכים, מגיע לשכבת האפיתליום (RPE) ושם חלקו נבלע. האור הנותר יעבור דרך הפוטורצפטורים לתחילת תהליך הראיה. תהליך הבליעה נועד להגן על שכבת הפוטורצפטורים מפני נזק פוטו-אוקסידטיבי, היכול להיגרם כתוצאה מכך שהרשתית חשופה לרמות גבוהות של אור בכל שעות היום.
בין שכבת תאי הגנגליון לקנים ולמדוכים יש שתי שכבות נוירופיל - רשתות שבהן מתבצעים הקשרים הסינפסיים. בשכבת הנוירופיל החיצונית מחוברים הקנים והמדוכים לתאים הביפולריים הפרושים במאונך ולתאים אופקיים שמתחברים לתאי הגנגליון.
פיזיולוגיה
מחלות רשתית
מחלות רבות פוגעות בתפקוד הרשתית, לחלקן יש טיפול רפואי בתרופות, הזרקות תוך עיניות או טיפול בלייזר, וחלקן מחייבות טיפול ניתוחי.
בצקת מקולרית על רקע סוכרת (רטינופתיה סוכרתית)
אחד מסיבוכי הסוכרת השכיחים הוא מחלת הרשתית בצקת מקולרית על רקע סוכרת, או בשם הפופולרי רטינופתיה סוכרתית. רטינופתיה סוכרתית פוגעת בעיקר בחולים "ותיקים" בסוכרת - מחלה המשפיעה על מערכות הגוף השונות, וביניהן כלי הדם הקטנים בגוף. מחלת רשתית זו נגרמת בשל זרימת דם מוגברת בכלי הדם ברשתית, עד כדי פגיעה בדופנותיהם. הדופנות הפגועות מפרישות נוזלים המצטברים בחלק האחורי של הרשתית ויוצרים בצקת, שפוגעת בראייה ומהווה סיכון משמעותי לעיוורון. בדיקות שגרה ואבחון מוקדם יוכלו להאט את קצב המחלה.[5]
ניוון מקולרי גילי (wAMD)
בניוון מקולרי גילי המחלה נגרמת כתוצאה מגדילה של כלי דם חדשים מתחת לפוביאה (שנמצאת במרכז המקולה). חלקם, כ-25%, חודרים מהדמית לתוך הרשתית ומדממים. מצב זה גורם בתוך זמן קצר לניוון ואובדן ראייה בחלקה הגדול של הפוביאה. הסיבה לדימומים נעוצה בכך שכלי הדם החדשים הם בעלי דופן חלשה יותר. כתוצאה מהדימום נוצרת רקמת צלקת במרכז הראייה הגורמת להופעת כתם שחור. ברוב המקרים המחלה מתבטאת בירידה בראייה המתבטאת באיבוד יכולת קריאה, יכולת אבחון פנים, יכולת קריאת שעון וראייה תפקודית. בדיקות לאבחון יוכלו לאתר את תהליך התפתחות המחלה טרם הופעת הסימפטומים.[6]
היפרדות רשתית
מצב בו רשתית העין נפרדת מקיר גלגל העין עקב קרע שנוצר בה. היפרדות רשתית מתרחשת כאשר הזגוגית נפרדת מחיבורה לרשתית. הזגוגית היא ג'ל הממלא את חלל העין. הג'ל הזה נהייה נוזלי עם הגיל, ובסופו של דבר ניתק מהחיבור הצמוד שלו לרשתית. כיום, קיים ניתוח להחזרת הרשתית שהופרדה. לניתוח זה אין 100% הצלחה, וקיימים ניתוחים שכשלו וגרמו לעיוורון של המנותח.
קרע/חור ברשתית

מצב בו קיים ברשתית העין חור, המגדיל את הסיכויים להיווצרות היפרדות הרשתית. סוג החור הנפוץ ביותר כיום נקרא "אופרקולום חופשי", בו החלק שנפרד בחור מרחף על פני זגוגית העין, ונקלט על ידי העין כעצמים צפים בעין, מעין לכלוכים או זבובים שחורים מעופפים באוויר. כיום, קיימת שיטה להלחמת החור או הקרע, באמצעות מכשיר לייזר ההופך אנרגיית אור לאנרגיית חום, ובעזרת החום "מלחים" את החור או הקרע. בכך נמנעת כניסה של ג'ל לעין המובילה להיפרדות רשתית.
CNV
צמיחת כלי דם פתולוגיים ברשתית במטופלים הסובלים מקוצר ראייה חמור (myopic CNV).
BRVO
בצקת מקולרית בעקבות חסימה בווריד הרשתית המרכזי (CRVO) או בסעיף וריד הרשתית (BRVO).
רטיניטיס פיגמנטוזה
רטיניטיס פיגמנטוזה (Retinitis pigmentosa) היא מחלת עיניים ניוונית של הרשתית, הנפוצה ביותר מבין מחלות ניוון הרשתית בעלות הורשה ברורה. תדירות המחלה נבדקה בעיקר בארצות-הברית ובאירופה ועומדת על אחד מתוך 4,000 אנשים. תדירות המחלה בישראל גבוהה יותר ובאזורים מסוימים עומדת על 1 מתוך 2,000 אנשים.
טיפול תרופתי במחלות רשתית
- אווסטין (Avastin) - תרופה אונקולוגית הפוגעת ביכולתו של הגידול הסרטני ליצור כלי דם. בשנת 2004 אושרה לחולי סרטן המעי הגס והרקטום ובמהלך השנים נרשמה באינדיקציות נוספות. החומר פועל על VEGF - ומונע את פעולתו ובכך מונע יצירת כלי דם חדשים. מאחר שלא נערך בה מחקר לטיפול בניוון מקולרי, היא אינה מאושרת על ידי ה-FDA או על ידי משרד הבריאות בישראל למטרה זו. למרות זאת, רופאים ומטופלים משתמשים בה בהצלחה על ידי הזרקתה בכמויות קטנות לעין.
- לוסנטיס (Lucentis) - תרופה דומה לאווסטין, עם מולקולה קטנה יותר, אשר פיתחה החברה המייצרת את האווסטין (נוברטיס). לוסנטיס קיבלה ביולי 2006 אישור של מנהל המזון והתרופות האמריקאי עבור טיפול ב-AMD רטוב.[7] ה-Lucentis יקרה פי 20 ויותר מן האווסטין (עקב עלות המחקרים וסיבות מסחריות), למרות שמדובר באותה מולקולה כמעט.
- אייליה (Eylea) אפליברספט - תרופה שפותחה במיוחד לטיפול במחלות רשתית, הרשומה לשימוש בישראל (כמו גם בארצות הברית ובאירופה) לטיפול בניוון מקולרי גילי, בצקת מקולרית על רקע סוכרת ומחלות רשתית נוספות.[8]
- לוקסטורנה (luxturna) תרופה שפותחה במיוחד לטיפול בגן RPE65 הגורם בין מאות גנים אחרים לרטיניטיס פיגמנטוזה. עברה את אישור ה-FDA בשנת 2017.[9]
חלק ממחלות הרשתית נגרמות בשל חלבון VEGF – חלבון המהווה "פקטור צמיחה" ומעודד צמיחה פתולוגית של כלי דם לא תקינים ברשתית. אייליה חוסמת את יכולתו של החלבון להיקשר לרצפטור שלו כשהיא נצמדת אליו משני צדדיו (כמו "שתי ידיים על הכדור")[10] באפיניות גבוהה פי 140 ויותר מתכשירים הנקשרים אל החלבון רק בצד אחד שלו. כתוצאה מכך ניתן להזריק אייליה בתדירות נמוכה יותר. בנוסף, אפליברספט לוכד גם את מולקולת PlGF (placental growth factor) שמעורבת אף היא בפתוגנזה של המחלה. בניוון מקולרי רשתי מטפלים באפליברספט בזריקות אחת לחודשיים (לאחר 3 מנות העמסה חודשיות). הפחתת תדירות ההזרקות תורמת להפחתה בסיכון לתופעות לוואי כתוצאה מזריקות עיניות, והפחתת העומס על הרופאים והמטופלים.
הבדלים ברשתית של בעלי חוליות וחסרי חוליות
סדר השכבות ברשתית של בעלי חוליות הוא "הפוך", בכך שהתאים הרגישים לאור נמצאים בצד האחורי של הרשתית, והאור צריך לעבור דרך שכבת נוירונים לפני שהוא פוגע בפוטורצפטורים. לעומת זאת, רשתית של חסרי חוליות בנויה בסדר הבא - הפוטורצפטורים הם בשכבה החיצונית של הרשתית, ומאחוריהם נמצאים הנוירונים המעבדים את האות. יתרונו של סידור זה הוא שהעצב האופטי המעביר את המידע אל המוח אינו גורם לאזור ריק מפוטורצפטורים, ולכן לבעלי חיים אלה אין כתם עיוור.
ראו גם
- ניוון מקולרי מחלת עיניים הפוגעת ברשתית
- בצקת מקולרית על רקע סוכרת
- חסימת וריד הרשתית המרכזי
- היפרדות רשתית
קישורים חיצוניים
- "כואב אבל פחות", גילה לוי-הוברמן, "ידיעות אחרונות" 17.11.2013
- ליאת רותם מלמד, בני 65? כך תצילו את הראייה שלכם, באתר ynet, 1 ביולי 2014
- פרופ' חנא גרזוזי, הטיפולים שמונעים עיוורון בקרב חולי סוכרת, באתר ynet, 14 באפריל 2015
- Reuters: Eylea works better vs Avastin and Lucentis in study
 אם היו מציעים לכם תרופה ב-50 דולר או ב-2,000 דולר, מה הייתם לוקחים?, באתר TheMarker, 8 בדצמבר 2014
אם היו מציעים לכם תרופה ב-50 דולר או ב-2,000 דולר, מה הייתם לוקחים?, באתר TheMarker, 8 בדצמבר 2014- רוני לינדר, מחקר: לוסנטיס יקרה פי 40 מאווסטין - אך יעילות התרופות זהה, באתר TheMarker, 2 במאי 2011
- מוסף בריאות העין, עמותת "לראות"
- רוני לינדר, התרופה לוסנטיס יקרה פי 40 מאווסטין - אך לא יעילה יותר, באתר הארץ, 4 באוקטובר 2010
- Kolb, H., Fernandez, E., & Nelson, R. (2003). The neural organization of the vertebrate retina. Salt Lake City, Utah: John Moran Eye Center, University of Utah. Retrieved July 19, 2004.
- Demo: Artificial Retina, MIT Technology Review, September 2004. Reports on implant research.
- Australian Vision Prosthesis Group, Graduate School of Biomedical Engineering, University of New South Wales.
- RetinaCentral, Genetics and Diseases of the Human Retina.
- Retinal layers image. NeuroScience 2nd Ed
- VisionSimulations.com | What the world looks like to people with various diseases and conditions of the eye
- The Organization of the Retina and Visual System
- Subretinal electronic chips allow blind patients to read letters and combine them to words
- S. Ramón y Cajal, Histologie du Système Nerveux de l'Homme et des Vertébrés, Maloine, Paris, 1911.
- M. Meister and M. J. B. II, The neural code of the retina, Neuron, vol. 22 p. 435-50, 1999.
- R. W. Rodieck, Quantitative analysis of cat retinal ganglion cell response to visual stimuli, Vision Research, vol. 5 p. 583-601, 1965.
- J. J. Atick and A. N. Redlich, What does the retina know about natural scenes?, Neural Computation, p. 196-210, 1992.
- Schulz, H., Goetz, T., Kaschkoetoe, J., Weber B.H. (2004). The Retinome - defining a reference transcriptome of the adult mammalian retina/retinal pigment epithelium - RetinaCentral. BMC Genomics. 2004 Jul 29;5(1):50. Institute of Human Genetics, Biocenter, University of Wuerzburg, D-97074 Wuerzburg, Germany. [email protected]
- Kevany, Brian M., and Krzysztof Palczewski. "Phagocytosis of retinal rod and cone photoreceptors." Physiology, 25.1, p.8-15, 2010.
- רשתית, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים
- ↑ ראו בקצרה תגובה לאור
- ↑ https://www.aao.org/bcscsnippetdetail.aspx?id=57bde6d0-29d1-4353-ae31-040769473b9d
- ↑ Webvision: The Organization of the Retina and Visual System, Color, Peter Gouras. Created: May 1, 2005; Last Update: July 1, 2009
- ↑ Foundations of Vision, Brian A. Wandell
- ↑ "רטינופתיה סוכרתית: גורמים", אתר "מכבי שירותי בריאות"
- ↑ "ניוון מקולרי גילי", אתר המרכז הרפואי "הדסה"
- ↑ ראו למשל דיווח חדשותי
- ↑ 12 33800 00&safa=h אישור ורישום אייליה, אגף הרוקחות במשרד הבריאות
- ↑ לוקסטורנה באתר הבית של החברה המייצרת.
- ↑ European Medicines Agency Summary for the public - Eylea
| מערכת הראייה האנושית | ||
|---|---|---|
| העין | רשתית • עדשה • קרנית • קשתית • אישון • תנועות עיניים | |
| מסלולים עצביים | עצב הראייה • תצלובת הראייה • גרעין הברך הצדי • קליפת הראייה • התליל העליון (Superior colliculus) • PPRF • FFA • MLF • FEF | |
| תאים ברשתית | תא קולט אור (קנים, מדוכים) • תא רשתית דו-קוטבי • תא גנגליון • תא אופקי • תא אמקרין | |
| תפיסה חזותית | ראייה • תפיסת עומק • תפיסת צבע • ראיית לילה • שדה ראייה • אשליה אופטית • הכתם העיוור | |
| אביזרים | משקפיים • תרשים לבדיקת ראייה • אוטורפרקטומטר • רטינוסקופ | |
הבהרה: המידע במכלול נועד להעשרה בלבד ואינו מהווה יעוץ רפואי.
רשתית42055163Q169342
