פורפירין
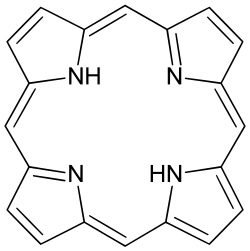
פּוֹרְפִירִינִים הם תרכובות אורגניות הטרוציקליות מאקרוציקליות (אנ') (בעלות טבעות עם מספר אטומים רב), המורכבות מארבע תת־יחידות פירול מותמרות, המחוברות באטומי הפחמן אלפא שלהן באמצעות גשרי מתין (אנ') (=CH−). בבעלי חוליות, חבר חיוני בקבוצת הפורפירינים הוא ההם, המהווה מרכיב בהמופרוטאינים (אנ'), שתפקידיהם כוללים נשיאת חמצן במחזור הדם. בצמחים, נגזרת פורפירין חיונית היא הכלורופיל, המעורב בקליטת אור (אנ') ובהעברת אלקטרונים בפוטוסינתזה.
תרכובת האב של הפורפירינים היא פורפין (אנ'), תרכובת כימית נדירה בעלת עניין תאורטי בלבד. פורפינים מותמרים נקראים פורפירינים.[1] עם סך של 26 אלקטרוני פאי, מבנה טבעת הפורפירין הוא מערכת ארומטית קואורדינטיבית.[2] תוצאה אחת של המערכת המצומדת הגדולה היא שפורפירינים בולעים בחוזקה בתחום הנראה של הספקטרום האלקטרומגנטי, כלומר הם בעלי צבע עמוק. השם "פורפירין" נגזר מיוונית πορφύρα (פורפירה), 'סגול'.[3]
מבנה
קומפלקסים של פורפירין מורכבים מליבת MN4 ריבועית מישורית. ההיקף של הפורפירינים, המורכב מפחמנים בהכלאת sp2, מציג בדרך כלל סטיות קטנות ממישוריות. פורפירינים "מרופטים" (ruffled) או בעלי צורת אוכף מיוחסים לאינטראקציות של המערכת עם סביבתה.[4] בנוסף, המתכת אינה ממוקמת לרוב במרכז מישור ה-N4.[5] עבור פורפירינים חופשיים, שני פרוטוני הפירול נמצאים בטראנס הדדי ובולטים מחוץ למישור ה-N4.[6] עיוותים לא-מישוריים אלה מקושרים לתכונות כימיות ופיזיקליות משתנות. טבעות כלורופיל הן באופן מובהק יותר לא-מישוריות, אך הן רוויות יותר מפורפירינים.[7]
קומפלקסים של פורפירינים
במקביל לעקירת שני פרוטוני N-H, פורפירינים קושרים יוני מתכת ב"כיס" ה-N4. ליון המתכת יש בדרך כלל מטען של 2+ או 3+. משוואה סכמטית לסינתזות אלה מוצגת להלן, כאשר M = יון מתכת ו-L = ליגנד:
- H2porphyrin + [MLn]2+ → M(porphyrinate)Ln−4 + 4 L + 2 H+
- פורפירינים מייצגים ונגזרותיהם
-
אוקטה-אתיל-פורפירין (אנ') (H2OEP) הוא אנלוג סינתטי של פרוטופורפירין IX. בניגוד לליגנדי הפורפירין הטבעיים, OEP2− הוא סימטרי במידה רבה.
-
טטרה-פניל-פורפירין (אנ') (H2TPP) הוא אנלוג סינתטי נוסף של פרוטופורפירין IX. בניגוד לליגנדי הפורפירין הטבעיים, TPP2− הוא סימטרי במידה רבה. הבדל נוסף הוא שמרכזי המתין (אנ') שלו תפוסים על ידי קבוצות פניל.
-
מבט מופשט על הם, קומפלקס של פרוטופורפירין IX.
-
ננו-טבעת של 40 מולקולות פורפירין, מודל.
-
ננו-טבעת של 40 מולקולות פורפירין, תמונת STM.
פורפירינים עתיקים
גאופורפירין, הידוע גם כפטרופורפירין, הוא פורפירין ממקור גאולוגי.[8] הם עשויים להימצא בנפט גולמי, פצלי שמן, פחם או סלעי משקע.[8][9] אבלסוניט (אנ') הוא כנראה המינרל הגאופורפיריני היחיד, שכן נדיר שפורפירינים מופיעים בנפרד ויוצרים גבישים.[10]
ראשיתו של תחום הגאוכימיה האורגנית (אנ') במיצוי פורפירינים מנפט. ממצאים אלה סייעו לבסס את המקורות הביולוגיים של הנפט.[11] נפט לעיתים "מזוהה" (fingerprinted) על ידי אנליזה של כמויות קורט של פורפיריני ניקל וונאדיל (אנ'). מטלופורפירינים באופן כללי הם תרכובות אורגניות יציבות מאוד, והמבנים המפורטים של הנגזרות שמוצו הבהירו שמקורם בכלורופיל.
ביוסינתזה
באאוקריוטים שאינם מבצעי פוטוסינתזה כגון בעלי חיים, חרקים, פטריות ופרוטוזואה, כמו גם בקבוצת החיידקים אלפא-פרוטאובקטריה (אנ'), השלב המחייב (אנ') לביוסינתזה (אנ') של פורפירין הוא יצירת חומצה דלתא-אמינו-לבולינית (אנ') (δ-ALA, 5-ALA או dALA) על ידי התגובה של חומצת האמינו גליצין עם סוקציניל-CoA (אנ') ממעגל קרבס. בצמחים, אצות, חיידקים (למעט קבוצת האלפא-פרוטאובקטריה) וארכאונים, הוא מיוצר מחומצה גלוטמית דרך גלוטמיל-tRNA וגלוטמט-1-סמיאלדהיד (אנ'). האנזימים המעורבים במסלול זה הם גלוטמיל-tRNA סינתטאז (אנ'), גלוטמיל-tRNA רדוקטאז (אנ'), וגלוטמט-1-סמיאלדהיד 2,1-אמינומוטאז (אנ'). מסלול זה ידוע כמסלול ה-C5 או מסלול ביל (Beale).
לאחר מכן, שתי מולקולות של dALA משולבות על ידי פורפובילינוגן סינתאז (אנ') לקבלת פורפובילינוגן (PBG), המכיל טבעת פירול. ארבע מולקולות PBG משולבות לאחר מכן באמצעות דיאמינציה להידרוקסי-מתיל-בילן (אנ') (HMB), שעובר הידרוליזה ליצירת הטטרה-פירול הטבעתי אורופורפירינוגן III (אנ'). מולקולה זו עוברת מספר שינויים נוספים. תוצרי ביניים משמשים במינים שונים ליצירת חומרים מסוימים, אך בבני אדם, התוצר הסופי העיקרי פרוטופורפירין IX (אנ') משולב עם ברזל ליצירת הם. פיגמנטי מרה (אנ') הם תוצרי הפירוק של ההם.
הסכמה שלהלן מסכמת את הביוסינתזה של פורפירינים, עם הפניות לפי מספר EC (אנ') ומסד הנתונים OMIM. הפורפיריה המקושרת למחסור בכל אנזים מוצגת גם היא:

סינתזה במעבדה

סינתזה נפוצה לפורפירינים היא תגובת רותמונד (אנ'), שדווחה לראשונה ב-1936, שהיא גם הבסיס לשיטות חדשות יותר שתוארו על ידי אדלר ולונגו (Adler and Longo).[12][13] הסכמה הכללית היא תהליך של תגובת דחיסה וחמצון המתחיל מפירול ואלדהיד.

יישומים פוטנציאליים
טיפול פוטודינמי
פורפירינים הוערכו בהקשר של טיפול פוטודינמי (PDT) מכיוון שהם בולעים אור בחוזקה, אשר מומר לאחר מכן לחום באזורים המוארים. טכניקה זו יושמה בניוון מקולרי באמצעות ורטפורפין (אנ').[14]
PDT נחשב לטיפול לא פולשני בסרטן, המערב אינטראקציה בין אור בתדירות מסוימת, פוטו-סנסיטייזר (חומר מעורר רגישות לאור), וחמצן. אינטראקציה זו מביאה ליצירת צורוני חמצן פעילים (אנ') (ROS) בעלי תגובתיות גבוהה, בדרך כלל חמצן סינגלט (אנ'), כמו גם אניון סופראוקסיד, רדיקל הידרוקסיל חופשי, או מי חמצן.[15] צורוני חמצן פעילים אלו מגיבים עם ביומולקולות אורגניות תאיות רגישות כגון ליפידים, חומצות אמינו ארומטיות, ובסיסים הטרוציקליים של חומצת גרעין, כדי לייצר רדיקלים מחמצנים הפוגעים בתא, ועשויים להשרות אפופטוזיס או אפילו נמק.[16]
אלקטרוניקה מולקולרית וחיישנים
תרכובות מבוססות-פורפירין מעוררות עניין כרכיבים אפשריים של אלקטרוניקה מולקולרית (אנ') ופוטוניקה.[17] צבעני פורפירין סינתטיים שולבו באבות-טיפוס של תאים סולאריים מרוגשי צבע (DSSC).[18][19]
יישומים ביולוגיים
פורפירינים נחקרו כתכשירים נוגדי דלקת אפשריים[20] והוערכו על פעילותם האנטי-סרטנית והנוגדת החמצון.[21] נמצא כי מספר מצומדי פורפירין-פפטיד הם בעלי פעילות אנטי-ויראלית נגד HIV בתנאי מעבדה (in vitro).[22]
טוקסיקולוגיה
הביוסינתזה של הם משמשת כסמן ביולוגי (אנ') במחקרי טוקסיקולוגיה סביבתית. בעוד שייצור עודף של פורפירינים מצביע על חשיפה לאורגנו-כלור (אנ'), עופרת מעכבת את האנזים ALA דהידראטאז (אנ').
גלריה
-
מבנה לואיס של מסו-טטרה-פניל-פורפירין
-
פורפירין משופעל-אור. חמצן חד-אטומי. הזדקנות תאית.
תרכובות קשורות
בטבע
מספר תרכובות הטרוציקליות הקשורות לפורפירינים נמצאות בטבע, כמעט תמיד קשורות ליוני מתכת. אלה כוללות:
| מאקרוציקלוס N4 | שם הקופקטור | מתכת | הערה |
|---|---|---|---|
| כלורין (אנ') | כלורופיל | מגנזיום | קיימות מספר גרסאות של כלורופיל (שייר צדדי; היוצא מן הכלל הוא כלורופיל c (אנ')) |
| בקטריוכלורין | בקטריוכלורופיל (אנ') (בחלקו) | מגנזיום | קיימות מספר גרסאות של בקטריוכלורופיל (שייר צדדי; חלקן משתמשות בטבעת כלורין רגילה) |
| סירוהידרוכלורין (אנ') (איזובקטריוכלורין) | סירוהם (אנ')Y | ברזל | קופקטור חשוב בהטמעת גופרית |
| תוצר ביניים ביוסינתטי בדרך לקופקטור F430 ו-B12 | |||
| קורין (אנ') | ויטמין B12 | קובלט | קיימות מספר גרסאות של B12 (שייר צדדי) |
| קורפין | קופקטור F430 (אנ') | ניקל | מאקרוציקלוס (אנ') מחוזר מאוד |
סינתטיים
בנזופורפירין הוא פורפירין בעל טבעת בנזן מאוחה לאחת מיחידות הפירול. לדוגמה, ורטפורפין (אנ') הוא נגזרת של בנזופורפירין.
איזומרים לא-טבעיים של פורפירין

איזומר הפורפירין הסינתטי הראשון דווח על ידי עמנואל פוגל (Emanuel Vogel) ועמיתיו ב-1986. איזומר זה, [18]פורפירין-(2.0.2.0), מכונה פורפיצן, וחלל ה-N4 המרכזי יוצר צורת מלבן כפי שמוצג באיור. פורפיצנים הראו התנהגות פוטופיזיקלית מעניינת ונמצאו כתרכובות רב-גוניות עבור טיפול פוטודינמי. תוצאה זו לוותה בהכנת [18]פורפירין-(2.1.0.1), שנקרא קורפיצן (corrphycene) או פורפיצרין (porphycerin). פורפירינים לא-טבעיים אחרים כוללים [18]פורפירין-(2.1.1.0) ו-[18]פורפירין-(3.0.1.0) או איזופורפיצן (isoporphycene). פורפירינים N-confused ("פורפירינים מבולבלים") מתאפיינים באחת מתת-יחידות הפירול כאשר אטומי החנקן פונים החוצה מליבת המאקרוציקלוס.[23]

קישורים חיצוניים
- פורפירין, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים
- ↑ Zhang, Wei; Lai, Wenzhen; Cao, Rui (2017). "Energy-Related Small Molecule Activation Reactions: Oxygen Reduction and Hydrogen and Oxygen Evolution Reactions Catalyzed by Porphyrin- and Corrole-Based Systems". Chemical Reviews. 117 (4): 3717–3797. doi:10.1021/acs.chemrev.6b00299. PMID 28222601.
- ↑ "Origin of aromatic character in porphyrinoid systems". Journal of Porphyrins and Phthalocyanines. 15 (11n12): 1093–1115. 2011. doi:10.1142/S1088424611004063.
- ↑ Harper D, Buglione DC. "porphyria (n.)". The Online Etymology Dictionary.
- ↑ Senge MO, MacGowan SA, O'Brien JM (בדצמבר 2015). "Conformational control of cofactors in nature - the influence of protein-induced macrocycle distortion on the biological function of tetrapyrroles". Chemical Communications. 51 (96): 17031–17063. doi:10.1039/C5CC06254C. PMID 26482230.
{{cite journal}}: (עזרה) - ↑ Walker FA, Simonis U (2011). "Iron Porphyrin Chemistry". Encyclopedia of Inorganic and Bioinorganic Chemistry. doi:10.1002/9781119951438.eibc0104. ISBN 978-1-119-95143-8.
- ↑ Jentzen W, Ma JG, Shelnutt JA (בפברואר 1998). "Conservation of the conformation of the porphyrin macrocycle in hemoproteins". Biophysical Journal. 74 (2 Pt 1): 753–763. Bibcode:1998BpJ....74..753J. doi:10.1016/S0006-3495(98)74000-7. PMC 1302556. PMID 9533688.
{{cite journal}}: (עזרה) - ↑ Senge MO, Ryan AA, Letchford KA, MacGowan SA, Mielke T (2014). "Chlorophylls, Symmetry, Chirality, and Photosynthesis". Symmetry. 6 (3): 781–843. Bibcode:2014Symm....6..781S. doi:10.3390/sym6030781.
- ^ 8.0 8.1 Kadish KM, ed. (1999). The Porphyrin Handbook. Elsevier. p. 381. ISBN 978-0-12-393200-6.
- ↑ Zhang B, Lash TD (בספטמבר 2003). "Total synthesis of the porphyrin mineral abelsonite and related petroporphyrins with five-membered exocyclic rings". Tetrahedron Letters. 44 (39): 7253. doi:10.1016/j.tetlet.2003.08.007.
{{cite journal}}: (עזרה) - ↑ Mason GM, Trudell LG, Branthaver JF (1989). "Review of the stratigraphic distribution and diagenetic history of abelsonite". Organic Geochemistry. 14 (6): 585. Bibcode:1989OrGeo..14..585M. doi:10.1016/0146-6380(89)90038-7.
- ↑ Kvenvolden, Keith A. (2006). "Organic geochemistry – A retrospective of its first 70 years". Organic Geochemistry. 37: 1–11. doi:10.1016/j.orggeochem.2005.09.001
- ↑ Rothemund P (1936). "A New Porphyrin Synthesis. The Synthesis of Porphin". J. Am. Chem. Soc. 58 (4): 625–627. Bibcode:1936JAChS..58..625R. doi:10.1021/ja01295a027.
- ↑ Rothemund P (1935). "Formation of Porphyrins from Pyrrole and Aldehydes". J. Am. Chem. Soc. 57 (10): 2010–2011. Bibcode:1935JAChS..57.2010R. doi:10.1021/ja01313a510.
- ↑ Wormald R, Evans J, Smeeth L, Henshaw K (ביולי 2007). "Photodynamic therapy for neovascular age-related macular degeneration" (PDF). The Cochrane Database of Systematic Reviews (3). doi:10.1002/14651858.CD002030.pub3. PMID 17636693.
{{cite journal}}: (עזרה) - ↑ Price M, Terlecky SR, Kessel D (2009). "A role for hydrogen peroxide in the pro-apoptotic effects of photodynamic therapy". Photochemistry and Photobiology. 85 (6): 1491–1496. doi:10.1111/j.1751-1097.2009.00589.x. PMC 2783742. PMID 19659920.
- ↑ Singh S, Aggarwal A, Bhupathiraju NV, Arianna G, Tiwari K, Drain CM (בספטמבר 2015). "Glycosylated Porphyrins, Phthalocyanines, and Other Porphyrinoids for Diagnostics and Therapeutics". Chemical Reviews. 115 (18): 10261–10306. doi:10.1021/acs.chemrev.5b00244. PMC 6011754. PMID 26317756.
{{cite journal}}: (עזרה) - ↑ Lewtak JP, Gryko DT (באוקטובר 2012). "Synthesis of π-extended porphyrins via intramolecular oxidative coupling". Chemical Communications. 48 (81): 10069–10086. doi:10.1039/c2cc31279d. PMID 22649792.
{{cite journal}}: (עזרה) - ↑ Walter MG, Rudine AB, Wamser CC (2010). "Porphyrins and phthalocyanines in solar photovoltaic cells". Journal of Porphyrins and Phthalocyanines. 14 (9): 759–792. doi:10.1142/S1088424610002689.
- ↑ Yella A, Lee HW, Tsao HN, Yi C, Chandiran AK, Nazeeruddin MK, et al. (בנובמבר 2011). "Porphyrin-sensitized solar cells with cobalt (II/III)-based redox electrolyte exceed 12 percent efficiency". Science. 334 (6056): 629–634. Bibcode:2011Sci...334..629Y. doi:10.1126/science.1209688. PMID 22053043. S2CID 28058582.
{{cite journal}}: (עזרה) - ↑ Alonso-Castro AJ, Zapata-Morales JR, Hernández-Munive A, Campos-Xolalpa N, Pérez-Gutiérrez S, Pérez-González C (במאי 2015). "Synthesis, antinociceptive and anti-inflammatory effects of porphyrins". Bioorganic & Medicinal Chemistry. 23 (10): 2529–2537. doi:10.1016/j.bmc.2015.03.043. PMID 25863493.
{{cite journal}}: (עזרה) - ↑ Bajju GD, Ahmed A, Devi G (בדצמבר 2019). "Synthesis and bioactivity of oxovanadium(IV)tetra(4-methoxyphenyl)porphyrinsalicylates". BMC Chemistry. 13 (1). doi:10.1186/s13065-019-0523-9. PMC 6661832. PMID 31384764.
{{cite journal}}: (עזרה) - ↑ Mendonça DA, Bakker M, Cruz-Oliveira C, Neves V, Jiménez MA, Defaus S, et al. (ביוני 2021). "Penetrating the Blood-Brain Barrier with New Peptide-Porphyrin Conjugates Having anti-HIV Activity". Bioconjugate Chemistry. 32 (6): 1067–1077. doi:10.1021/acs.bioconjchem.1c00123. PMC 8485325. PMID 34033716.
{{cite journal}}: (עזרה) - ↑ Hiroyuki F (1994). ""N-Confused Porphyrin": A New Isomer of Tetraphenylporphyrin". J. Am. Chem. Soc. 116 (2): 767. Bibcode:1994JAChS.116..767F. doi:10.1021/ja00081a047.
פורפירין42728413Q422926









